Кристаллическая атомная решетка примеры
Содержание
Многообразие физико-химических свойств веществ во многом определяются их пространственным строением при заданных температурах и давлениях.
Примером может быть вода, которая при разных температурах меняет свое агрегатное состояние от газообразного (пар) до твердого (лед), имеющего кристаллическую решетку. Благодаря ей твердые вещества обладают формой и объемом, имеют определенные физические характеристики.
Однако, существует класс веществ-элементов, которым не свойственен процесс кристаллизации — упорядоченной пространственной структуры. Их называют аморфными.
Основные данные
Кристаллическая решетка (КР) является виртуально-вспомогательным образом, помогающим анализировать и описывать построение 3D-структур.
Она образована совокупностью частиц, располагаемых в ее узлах и для каждой точки расположение остальных симметрично и одинаково. В зависимости от соединения, эти узлы могут быть атомами, ионами или молекулами. При анализе точку совмещают с их центрами или элементом симметрии.
Удержание пространственно-структурных особенностей обеспечивается химическим взаимодействием между центрами. Такие взаимодействия могут быть:
- атомными (ковалентное взаимодействие);
- металлическими (металлические виды связывания);
- межмолекулярными;
- катион-анионными.
Типы кристаллических решеток в химии
Существуют основные типы кристаллических решеток — пространственной организации твердой материи, во многом определяющей ее физико-химические параметры.
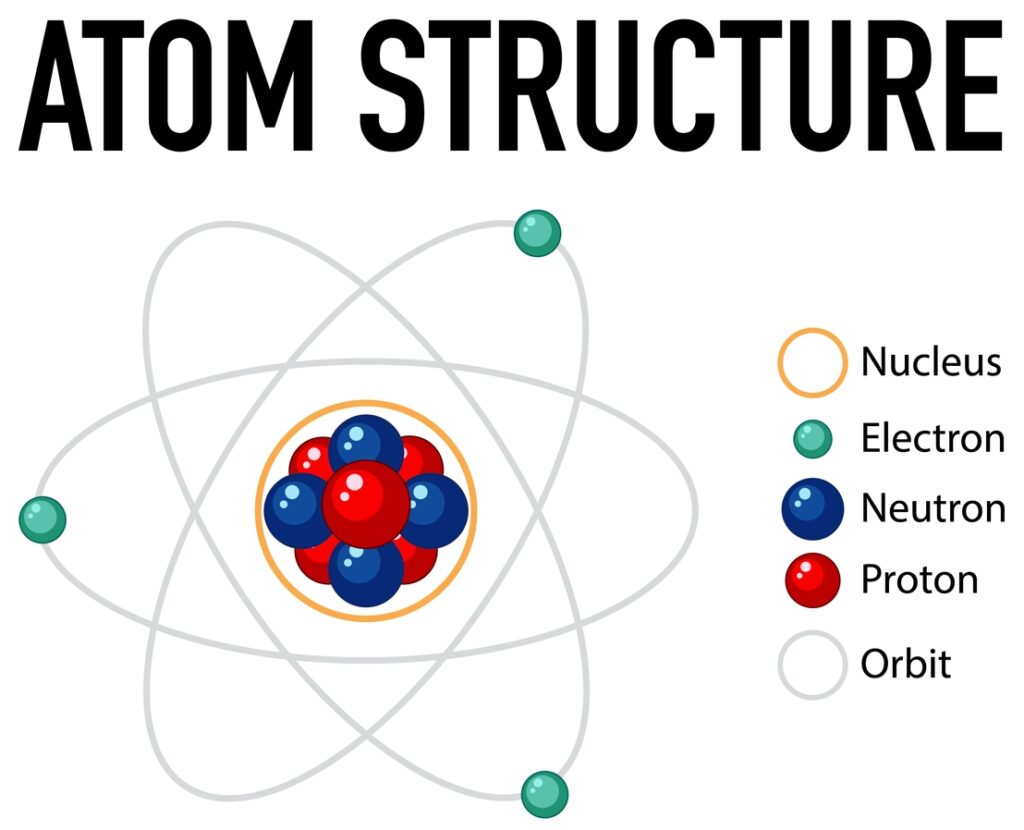
Кристаллическая атомная решетка
Пространственная организация, в которой ковалентное взаимодействие удерживает атомарные центы, с передачей соседствующим атомам электрон-корпускул. Такие 3D-структуры очень устойчивые, что определяет физико-химические параметры соединений и характеризующихся:
- отличными прочностными характеристиками;
- отсутствием летучести;
- нерастворимостью;
- высокими температурами расплавления и закипания.
Веществами с атомными кристаллическими решетками могут быть: алмазы, кристаллы бора, графит и т.д.

Кристаллические решетки молекулярные
В ней частицей, образующей узел, является молекула, которая притягивается к соседним молекулам слабым межмолекулярным притяжением.
При комнатных температурах они газообразные, легкокипящие жидкости или легкоплавкие твердые вещества. Легко отрываемые молекулы обеспечивают их летучесть и появление характерного запаха. Пространственной структурой объясняется возгонка — твердое вещество переходит в газ, без жидкостной фазы.
К свойствам молекулярных кристаллических решеток относят:
- небольшие показатели твердости и прочности;
- подверженность возгонке;
- высокие уровни легко-плавкости;
- присутствие запахов и явление летучести.
Соединения и элементы с кристаллическими решетками молекулярными примеры: жидкая вода, белый фосфор, йод, кислород, органические комплекса и т.д.
Ионная КР
Одним из видов решеток кристаллических являются ионная КР, с расположенными в центрах ионами с различным зарядом.
Связи образуются при передаче атомом ионов другому атому с появлением разно-заряженных пар, между которыми возникает электрическое притяжение. Эти пары образуют структуру кристалла.
Представители этого типа характеризуются:
- твердостью;
- электропроводностью;
- хрупкостью;
- нелетучестью;
- тугоплавкостью;
- водорастворимостью.
Типичным примером ионной кристаллической решетки можно считать кристаллы поваренной соли NaCl, она присутствует у щелочей и оксидов активных металлов.
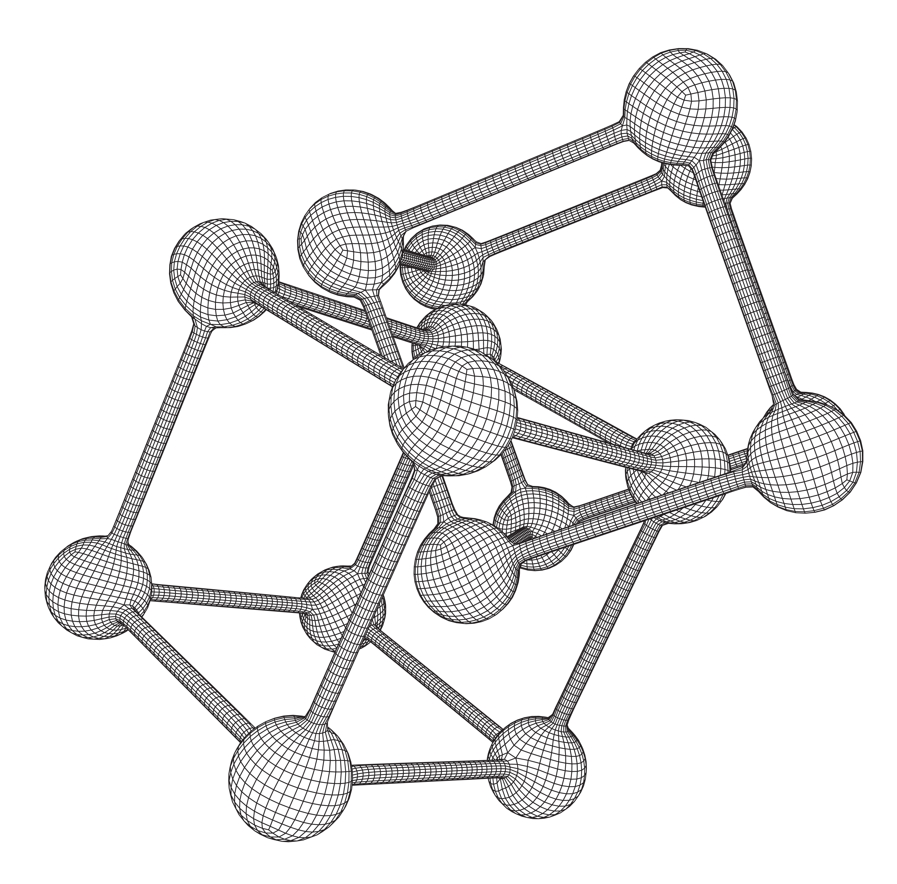
Металлическая КР
Для того, чтобы понять металлическая кристаллическая решетка что такое, нужно вспомнить механизм образования металлохимической связи. В ней перемещаемый электронный газ свободно движется внутри структуры.
Содержащиеся в нем электроны присоединяются к положительным ионам, образуя атомы. Или отщепляются от них, продолжая свободное движение. В этом типе кристаллов происходит непрерывное разрушение атомарных структур и образование новых. Такие КР характеризуют металлы и образуемые ими сплавы.
Электронный газ хаотично передвигается внутри твердых тел, но при возникновении разницы потенциалов, начинает упорядоченное передвижение, что объясняет явление проводимости.
Отличительные свойства:
- присутствие характерного блеска и высокой теплопроводности;
- подверженность механической обработке и хорошей пластичности, ковкости;
- отлично проводят электроток.
Элементы и их сплавы значительно различаются температурой плавления. Кристаллическая решетка металлов претерпевает значительные изменения при введении в их состав других присадок, меняя физико-химические характеристики.
